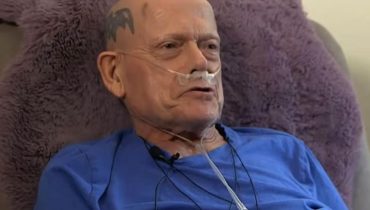
📌 Doliprane enfants : 27 lots rappelés à cause de pipettes défectueuses qui risquent de provoquer des surdosages
Posted 24 février 2026 by: Admin
Un Rappel D’urgence Qui Touche Les Familles Françaises
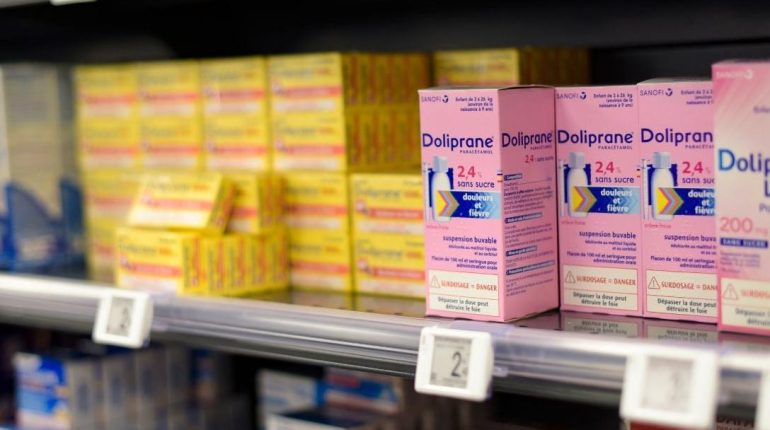
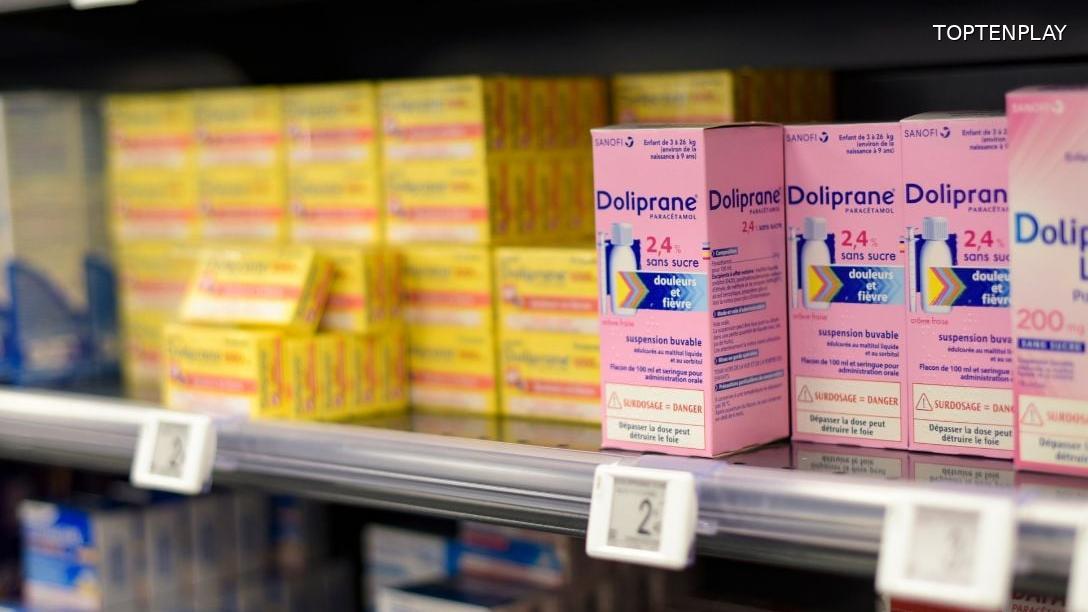
Le 23 février 2026, l’Agence nationale de sécurité du médicament et des produits de santé a ordonné le retrait immédiat de 27 lots de Doliprane 2,4 % suspension buvable, le sirop au paracétamol présent dans des milliers de foyers français. Cette décision concerne exclusivement la forme destinée aux nourrissons et jeunes enfants pesant entre 3 et 26 kg, un produit administré quotidiennement pour soulager fièvres, poussées dentaires et rhumes.
Les lots visés, numérotés de L033 à L062, ont été distribués dans les pharmacies françaises entre le 12 novembre 2025 et le 3 février 2026. Leurs dates de péremption s’échelonnent d’août à octobre 2027, suggérant qu’une quantité significative de flacons se trouve encore dans les armoires à pharmacie familiales. L’ANSM invite les parents à vérifier immédiatement le numéro de lot inscrit sur le flacon ou au dos de la boîte, puis à consulter la liste complète publiée sur son site Internet.
Cette mesure intervient après l’identification d’un défaut de fabrication spécifique qui, bien que ne remettant pas en cause la qualité du médicament lui-même, soulève des préoccupations légitimes quant à la sécurité d’usage chez les plus vulnérables.
Un Défaut De Fabrication Ciblé Sur La Pipette Doseuse
L’origine du problème ne réside pas dans le sirop au paracétamol, dont la composition et l’efficacité demeurent intactes. L’ANSM pointe précisément un défaut technique affectant les graduations de la pipette doseuse fournie avec les flacons concernés. Ces repères de mesure, essentiels pour administrer la dose exacte selon le poids de l’enfant, présentent une faiblesse de conception inattendue.
« Les graduations de certaines pipettes fournies avec les flacons de Doliprane 2,4 % suspension buvable sont susceptibles de s’effacer progressivement, après un rinçage à l’eau tiède ou chaude », détaille l’agence sanitaire dans son communiqué. Ce phénomène d’effacement transforme un dispositif médical de précision en instrument potentiellement trompeur pour les parents qui, en toute bonne foi, pourraient administrer des quantités inexactes.
Seule la forme suspension buvable 2,4 % est visée par ce rappel. Les comprimés, gélules, sachets, suppositoires et autres dosages pédiatriques de la gamme Doliprane restent disponibles sans restriction. Les autorités insistent sur la distinction capitale entre le contenant défectueux et le contenu irréprochable, une nuance cruciale pour éviter toute confusion dans les foyers français.
Ce défaut de fabrication, bien que circonscrit à un seul site de production désormais identifié et corrigé, soulève néanmoins des interrogations quant aux conséquences d’un mauvais dosage répété chez les tout-petits.
Les Risques Réels D’Un Surdosage En Paracétamol
Ces interrogations trouvent leur réponse dans les mécanismes physiologiques du surdosage en paracétamol chez les nourrissons. L’ANSM explicite sans détour les conséquences d’une administration excessive : « Ce défaut qualité peut ensuite entraîner une erreur dans le dosage du médicament avec un risque potentiel de surdosage en paracétamol » chez les enfants de 3 à 26 kg.
Le paracétamol, molécule réputée pour sa sécurité lorsqu’il est correctement dosé, révèle un visage autrement plus préoccupant en cas d’excès. Les autorités sanitaires rappellent qu’un surdosage « peut causer des lésions du foie » chez les tout-petits, dont l’organisme immature métabolise différemment ce principe actif. L’accumulation progressive de doses trop élevées, même légèrement supérieures aux recommandations, sollicite excessivement les cellules hépatiques encore fragiles des jeunes enfants.
Cette mise en garde prend une dimension rassurante lorsqu’on examine les faits vérifiés : aucun effet indésirable en lien avec ce défaut n’a été signalé au laboratoire Opella Healthcare France à ce jour. L’absence de cas avérés suggère que le rappel intervient suffisamment tôt pour prévenir toute complication, transformant cette alerte en démonstration d’une surveillance pharmaceutique efficace.
La rapidité de cette intervention préventive permet désormais aux familles de suivre une procédure claire pour sécuriser définitivement l’administration du traitement.
Procédure De Remplacement Et Garanties D’Approvisionnement
Cette sécurisation passe d’abord par une vérification simple mais essentielle : examiner le numéro de lot inscrit sur le flacon ou au dos de la boîte. Les parents doivent rechercher les références comprises entre L033 et L062, correspondant aux lots distribués du 12 novembre 2025 au 3 février 2026, avec des dates de péremption s’échelonnant d’août à octobre 2027.
L’ANSM établit trois consignes sans ambiguïté pour les familles concernées : ne plus utiliser la pipette fournie avec un lot identifié, ne pas la remplacer par celle d’un autre médicament, et rapporter l’ensemble en pharmacie pour obtenir un échange gratuit. Cette procédure, qualifiée de « mesure de précaution » par les autorités, permet un remplacement immédiat sans frais pour les patients.
La question de la disponibilité du traitement trouve une réponse formelle du ministère de la Santé : « La couverture des besoins reste assurée sans ces lots ». Opella Healthcare France confirme que les stocks disponibles suffisent à prévenir toute rupture d’approvisionnement, écartant le scénario de pénurie redouté lors de précédentes alertes sanitaires.
Les autorités apportent une précision technique révélatrice sur la résolution du problème : l’origine du défaut a été localisée sur un site de production spécifique, où les corrections nécessaires ont depuis été appliquées. Les pipettes fabriquées sur les autres sites n’ont présenté aucune anomalie, garantissant la fiabilité des nouveaux flacons distribués.