📌 Le cytomégalovirus, nouvelle cible dans la lutte contre le glioblastome
Posted 3 mai 2026 by: Admin
Chaque année, des milliers de patients reçoivent le diagnostic d’un glioblastome, la tumeur cérébrale la plus fréquente et la plus agressive chez l’adulte, dont la survie moyenne dépasse rarement dix-huit mois après le diagnostic. Depuis plus de vingt ans, des chercheurs explorent une piste inattendue : le rôle du cytomégalovirus humain (CMVH), un virus présent dans l’organisme de plus d’un adulte sur deux, dans l’évolution de cette tumeur. Si le virus n’en serait pas à l’origine, il pourrait en amplifier l’agressivité — et, surtout, représenter une nouvelle cible thérapeutique.
En bref
- —Le glioblastome tue en moyenne en 18 mois malgré les traitements
- —Un virus courant amplifie l’agressivité de la tumeur sans en être la cause
- —Des antiviraux existants montrent des résultats préliminaires encourageants
Le glioblastome, une tumeur cérébrale au pronostic encore très sombre
Le glioblastome est un gliome — une tumeur qui prend naissance dans le tissu de soutien du cerveau, les cellules gliales, et plus précisément dans les astrocytes et les oligodendrocytes. Sa croissance est rapide et infiltrante, ce qui rend son retrait chirurgical complet quasi impossible.
Bien que relativement rare — on recense 2 à 5 cas pour 100 000 personnes dans le monde —, le glioblastome est le cancer cérébral primaire le plus fréquent chez l’adulte. Son incidence modeste en valeur absolue contraste avec la sévérité du pronostic qu’il impose.
Malgré la combinaison des traitements standards — chirurgie d’exérèse, radiothérapie ciblée et chimiothérapie —, la survie médiane après le diagnostic reste d’environ dix-huit mois, et peu de patients survivent au-delà de cinq ans. Cette résistance persistante aux thérapies classiques en fait un enjeu majeur de santé publique, mobilisant des équipes de recherche dans le monde entier.
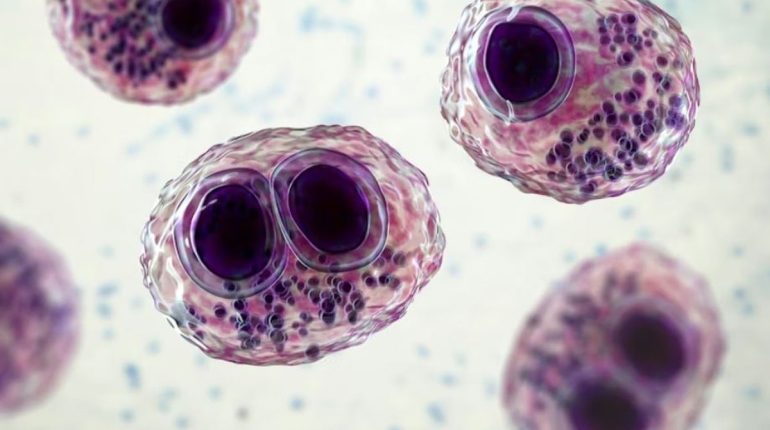
Le cytomégalovirus, un virus discret aux effets insoupçonnés
Le cytomégalovirus humain (CMVH) appartient à la même grande famille virale que l’herpès labial ou le virus de la varicelle : les Herpesviridae. Il circule discrètement dans la population mondiale : dans de nombreux pays, plus d’un adulte sur deux a déjà été exposé au virus, souvent sans le savoir, la primo-infection étant généralement asymptomatique.

Après cette première rencontre avec le système immunitaire, le CMVH ne disparaît pas. Il s’installe dans certaines cellules de l’organisme sous une forme latente, prêt à se réactiver lorsque les défenses immunitaires fléchissent. Cette caractéristique est commune à l’ensemble des herpèsvirus.
Ce qui distingue le CMVH, c’est sa capacité à modifier le fonctionnement des cellules qu’il infecte. Le virus peut stimuler leur prolifération, les protéger contre la mort cellulaire programmée et interférer avec la réponse immunitaire locale. Des propriétés qui, en contexte tumoral, pourraient avoir des conséquences importantes sur l’évolution de la maladie.
L’oncomodulation : comment le virus amplifie l’agressivité de la tumeur
Le lien entre CMVH et glioblastome ne date pas d’hier. Au début des années 2000, des équipes de recherche ont détecté pour la première fois de l’ADN viral et des protéines spécifiques du cytomégalovirus dans des échantillons de tumeurs cérébrales. Depuis, ces observations ont été confirmées par de nombreux laboratoires à travers le monde.

La quantité de virus détectée dans les cellules tumorales reste faible — bien en deçà de ce que l’on observe lors d’une infection active. Pourtant, même à ces niveaux, le CMVH produit des protéines capables d’influencer le comportement des cellules cancéreuses. Il n’est pas considéré comme la cause du glioblastome, mais comme un « oncomodulateur » : un agent qui ne déclenche pas la tumeur, mais en amplifie les caractéristiques les plus dangereuses.
Les mécanismes impliqués sont multiples. L’infection par le CMVH favorise la formation de nouveaux vaisseaux sanguins autour de la tumeur — un processus appelé angiogenèse —, permettant à celle-ci de s’alimenter plus efficacement. Le virus inhibe également l’apoptose, ce mécanisme naturel d’élimination des cellules anormales, et modifie le métabolisme cellulaire au profit de la survie tumorale. Il contribue enfin à créer un environnement local hostile au système immunitaire, réduisant la capacité de l’organisme à combattre la maladie.
En 2025, le Centre international de recherche sur le cancer (CIRC/IARC) a officiellement classé le CMVH dans le groupe 2B, le reconnaissant comme « probablement cancérogène pour l’humain ». Cette décision a renforcé l’attention scientifique portée à ses effets sur la progression tumorale.
Le CMVH classé cancérogène probable en 2025
En 2025, le Centre international de recherche sur le cancer (CIRC) a officiellement classé le cytomégalovirus humain dans le groupe 2B, soit « probablement cancérogène pour l’humain ». Cette décision s’appuie sur l’accumulation de données scientifiques reliant le virus à plusieurs types de tumeurs. Le CMVH est par ailleurs la principale cause d’infection transmise de la mère à l’enfant pendant la grossesse, ce qui soulève des questions sur son rôle potentiel dans certaines tumeurs pédiatriques.
Antiviraux, immunothérapie et peptides : les nouvelles pistes qui se dessinent
La présence du CMVH dans les glioblastomes a conduit à explorer des traitements antiviraux comme approche complémentaire. Des études pilotes ont été menées avec le valganciclovir, un médicament déjà utilisé en clinique contre les infections à cytomégalovirus. Bien que les résultats restent préliminaires et nécessitent des confirmations à plus grande échelle, certains patients ont présenté une amélioration relative de leur survie.

En parallèle, la recherche explore des approches d’immunothérapie ciblant spécifiquement le virus. L’objectif est d’entraîner le système immunitaire à reconnaître et détruire les cellules tumorales qui expriment des protéines virales. Cette stratégie ouvre une voie complémentaire aux traitements classiques, aujourd’hui encore insuffisants pour contrôler la maladie sur le long terme.
Une troisième piste émerge également : celle des petits peptides. Ces molécules sont conçues pour bloquer l’interaction entre deux protéines essentielles à la réplication du virus, l’empêchant ainsi de se multiplier au sein des cellules tumorales. Cette approche, encore au stade expérimental, pourrait à terme compléter ou remplacer les antiviraux classiques, dont l’efficacité peut être limitée par l’apparition de résistances.
Le concept d’oncomodulation ne se limite pas au glioblastome. Des chercheurs envisagent son application à d’autres cancers potentiellement influencés par le CMVH, y compris certaines tumeurs pédiatriques comme le médulloblastome. La question du rôle de l’infection congénitale — transmise de la mère à l’enfant pendant la grossesse — dans la modulation tumorale représente un axe de recherche encore largement inexploré.
Le glioblastome reste, en 2026, l’un des cancers les plus difficiles à traiter. Mais la piste du cytomégalovirus humain, progressivement consolidée depuis plus de vingt ans de recherche, ouvre aujourd’hui des perspectives concrètes : agir non seulement sur la tumeur elle-même, mais aussi sur le virus qui en amplifie l’agressivité. Des essais cliniques plus larges sont encore nécessaires pour valider l’efficacité des approches antivirales et immunothérapeutiques. Si ces résultats se confirment, ce changement de paradigme — considérer une infection virale comme levier thérapeutique dans un cancer — pourrait redéfinir la prise en charge du glioblastome et, au-delà, influencer l’ensemble de la recherche oncologique.




















