À 6 ans, Saffie Sandford voyait à peine dans la pénombre — une condition qui menaçait de la plonger dans la cécité complète à l’âge adulte. Deux injections d’une thérapie génique de pointe, le Luxturna, ont transformé son quotidien au point que sa mère évoque une « baguette magique ». Une avancée que vient de confirmer une étude publiée dans JAMA Ophthalmology, montrant pour la première fois que ce traitement renforce également les voies visuelles du cerveau chez le jeune enfant.
En bref
- —Saffie, 6 ans, peut désormais voir dans l’obscurité
- —7 enfants sur 10 montrent des améliorations mesurables dans l’étude
- —Le Luxturna coûte environ 850 000 dollars par patient
Une enfance dans l’obscurité : le quotidien d’une fillette atteinte d’ACL
C’est à l’âge de 5 ans que les médecins de l’hôpital Moorfields, à Londres, posent le diagnostic : Saffie Sandford, originaire de Stevenage, dans le Hertfordshire, est atteinte d’une amaurose congénitale de Leber (ACL), une maladie génétique rare touchant la rétine. En cause, une mutation dans les deux copies du gène RPE65, indispensable au fonctionnement des cellules visuelles.
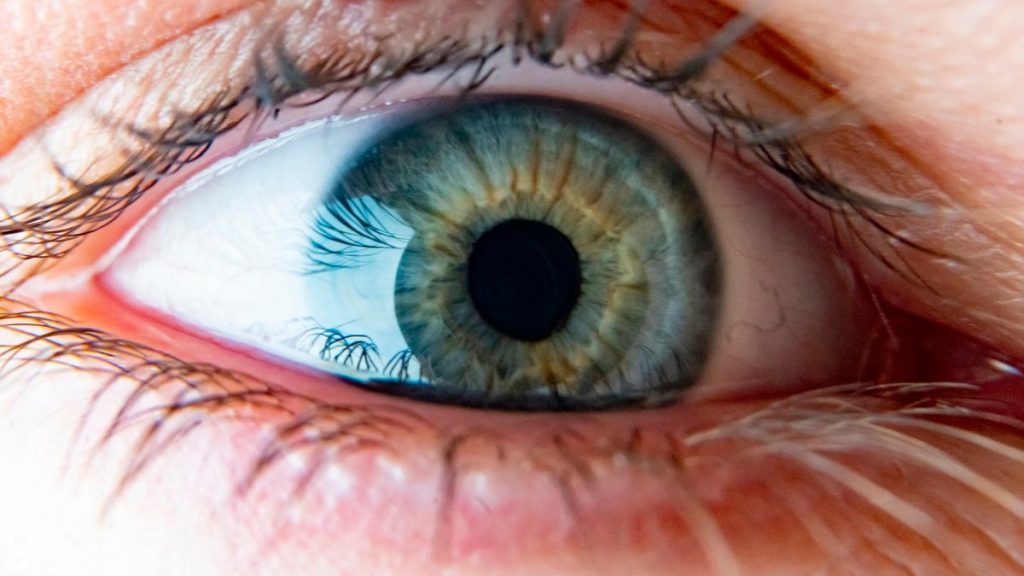
L’ACL se manifeste dès la naissance par une vision très limitée en pleine lumière, et une cécité quasi totale dans la pénombre. Sans traitement, la maladie évolue inexorablement vers une perte totale de la vue à l’âge adulte. Pour la mère de Saffie, le constat était sans équivoque : sa fille était, selon ses propres mots, « totalement aveugle dans l’obscurité ».
Les conséquences sur la vie quotidienne de la fillette étaient multiples. Incapable de se repérer dans un environnement peu éclairé ou de jouer sur une aire de jeux sans risquer de se blesser, Saffie voyait également ses résultats scolaires affectés par cette déficience. C’est dans ce contexte que les médecins de Great Ormond Street Hospital (GOSH), à Londres, lui ont proposé d’accéder au programme de thérapie génique Luxturna, disponible dans le cadre du système de santé britannique.
L’amaurose congénitale de Leber : une maladie rare et sévère
L’amaurose congénitale de Leber est l’une des formes les plus graves de dystrophie rétinienne héréditaire : elle se déclare dès la naissance et évolue progressivement vers la cécité à l’âge adulte. Elle résulte de mutations dans différents gènes impliqués dans le fonctionnement de la rétine. La forme liée au gène RPE65 — dont est atteinte Saffie — est la seule pour laquelle un traitement approuvé existe à ce jour.
Luxturna : comment une injection dans l’œil peut réparer un gène défaillant
Le Luxturna — nom commercial du voretigène néparvovec — repose sur un principe élégant : un virus inoffensif, modifié en laboratoire, sert de vecteur pour transporter une copie saine du gène RPE65 directement sous la rétine du patient. Une fois en place, ce gène permet aux cellules rétiniennes de produire à nouveau la protéine manquante et de rétablir une partie du signal visuel.
Saffie a reçu une première injection dans un œil en avril 2025, puis une seconde dans l’œil opposé en septembre 2025, à GOSH. Les résultats ne se sont pas fait attendre. Progressivement, la fillette a commencé à distinguer son environnement dans la pénombre, à repérer des obstacles à sa périphérie, et à participer à des activités jusqu’alors hors de portée.
Sa mère décrit la transformation avec une émotion palpable : « C’est comme si quelqu’un avait agité une baguette magique et lui avait rendu la vue dans l’obscurité. » La vision périphérique de Saffie, quasi inexistante avant le traitement, s’est également améliorée de façon significative — lui permettant, pour la première fois, de grimper seule sur une structure de jeu.
Ce que révèle l’étude GOSH/UCL publiée dans JAMA Ophthalmology
Le cas de Saffie n’est pas un cas isolé. Des chercheurs de GOSH et de l’University College London (UCL) ont suivi 15 enfants traités par Luxturna entre 2020 et 2023, âgés de 15 mois à 12 ans. Leurs résultats, publiés dans JAMA Ophthalmology, apportent une preuve scientifique inédite de l’impact du traitement au-delà de la rétine.

Pour mesurer cet impact, les chercheurs ont utilisé les potentiels évoqués visuels (VEP), un test non invasif qui mesure les signaux électriques transmis de la rétine jusqu’au cortex visuel du cerveau. Sur les enfants ayant pu compléter les évaluations, 7 sur 10 présentaient des améliorations cliniquement significatives. C’est donc le câblage neurologique de la vision lui-même qui se renforce sous l’effet du traitement.
La découverte la plus importante concerne l’âge de prise en charge. Les nourrissons et très jeunes enfants traités durant la fenêtre critique du développement visuel affichent les progrès les plus marquants. « Pour la première fois, nous avons pu démontrer objectivement que la thérapie génique peut renforcer les voies visuelles du cerveau chez de très jeunes enfants », souligne le Dr Rob Henderson, ophtalmologiste consultant à GOSH. Ce résultat plaide fortement pour un dépistage et une intervention précoces.
Un espoir immense, mais des obstacles réels
Malgré l’enthousiasme suscité par ces résultats, les médecins maintiennent une posture prudente. Le Luxturna n’est pas présenté comme un traitement curatif définitif : la durée des effets reste à ce jour incertaine, et aucune donnée ne garantit que les améliorations perdurent sur le très long terme. La mère de Saffie elle-même le reconnaît : « Nous savons que cela ne durera peut-être pas, mais nous nous sentons chanceux chaque jour qu’elle ait eu cette opportunité. »

Le principal obstacle à la diffusion de cette thérapie reste son coût : environ 850 000 dollars par patient, ce qui en fait l’un des médicaments les plus chers au monde. Au Royaume-Uni, le traitement est accessible via le NHS, le système de santé public britannique — ce qui a permis à Saffie d’y accéder sans frais directs pour sa famille.
En France, le Luxturna a reçu une autorisation de la Haute Autorité de Santé (HAS), mais son usage est strictement réservé à l’hôpital, dans des centres experts spécialisés. Les conditions réelles de prise en charge par l’Assurance maladie restent l’objet de discussions, dans un contexte où le prix des thérapies géniques soulève un débat croissant sur l’équité d’accès aux innovations médicales.
Sur le plan scientifique, des essais cliniques sont par ailleurs en cours pour d’autres formes génétiques d’amaurose congénitale de Leber, notamment grâce à l’édition du génome par CRISPR-Cas9. Ces approches pourraient, à terme, ouvrir des perspectives thérapeutiques pour les patients porteurs de mutations aujourd’hui sans traitement disponible.
L’histoire de Saffie résume à elle seule les promesses et les limites de la révolution génomique en cours. Pour des enfants atteints d’une maladie rare et dévastatrice, le Luxturna ouvre une fenêtre d’espoir réelle — à condition d’intervenir tôt, et d’avoir accès au traitement. L’étude de GOSH et de l’UCL marque une étape scientifique majeure en prouvant, pour la première fois, que la thérapie peut agir jusqu’aux voies visuelles du cerveau lui-même. Reste entière la question de l’accès : comment garantir que ces avancées bénéficient au plus grand nombre, et non aux seuls pays dont le système de santé peut absorber un coût aussi exorbitant ?